Hoà tan hết 2,3g Na kim loại vào 97,8g nước thu được dung dịch có nồng độ:
A. 2,4%
B. 4,0%
C. 23,0%
D. 5,8%
Hoà tan hết 2,3g Na kim loại vào 97,8g nước thu được dung dịch có nồng độ:
A. 2,4%
B. 4,0%
C. 23,0%
D. 5,8%

C % N a O H = m N a O H m dd .100 % = 0,1.40 100 .100 % = 4 % .
Đáp án B
Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng
hoà tan hết 2,3g Na kim loại vào 97,8g nước thu được dd có nồng độ bao nhiêu?
Sửa lại :
nNa=0,1
2Na+2H2O-->2NaOH+H2
0,1-----------------0,1-------0,05
=>Cm NaOH=0,1/0,0978=1,02M
mNaOH=4g
=>C% NaOH=4*100/(2,3+97,8-0,05*2)=4%
Na + H2O ==> NaOH + 1/2H2
0.1==>> 0.1=>0.05
==>> C%=3.3%
Cho 2,3 gam Na vào 100g dd NaOH 10%. Tính nồng độ phần trăm và nồng độ mol/lít của dd mới. Biết khối lượng riêng của dung dịch mới là 1,05 g/ml
PTHH: 2Na + 2H2O -> 2NaOH + H2↑
\(n_{Na}=\dfrac{2.3}{23}=0.1\left(mol\right)\)
\(m_{NaOH\left(10\%\right)}=100\cdot10\%=10\left(g\right)\)
\(n_{NaOH\left(10\%\right)}=\dfrac{10}{40}=0.25\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(0.1......................0.1..........0.05\)
\(\sum n_{NaOH}=0.25+0.1=0.35\left(mol\right)\)
\(m_{NaOH}=0.35\cdot40=14\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=2.3+100-0.05\cdot2=102.2\left(g\right)\)
\(C\%_{NaOH}=\dfrac{14}{102.2}\cdot100\%=13.7\%\)
\(V_{dd}=\dfrac{102.2}{1.05}=97.33\left(ml\right)=0.0973\left(l\right)\)
\(C_{M_{NaOH}}=\dfrac{0.35}{0.0973}=3.6\left(M\right)\)
Hoà tan m1 g Na vào m2g H2O thu được dung dịch B có tỉ khối d. Khi đó có phản ứng: 2Na+ 2H2O -> 2NaOH + H2
a/ Tính nồng độ % của dung dịch B theo m.
b/ Tính nồng độ mol của dung dịch B theo m và d.
c/ Cho C% = 16% . Hãy tính tỉ số m1/m2.. Cho CM = 3,5 M. Hãy tính d.
Hoà tan hoàn toàn 5,8 gam hỗn hợp gồm kim loại M và oxit của nó vào nước, thu được 1 lít dung dịch chứa một chất tan có nồng độ 0,04M và 0,448 lít khí H2 (đktc). Kim loại M là
A. Na.
B. Ba.
C. Ca.
D. K.
Chọn B.
Hỗn hợp 5,8 gam có M (a mol) và M2Ox (b mol) Þ Ma + (2M + 16x).b = 5,8 (1)
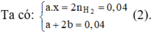
Với x = 1 hoặc 2 thay vào (1), (2) suy ra M = 137 (Ba)
Hoà tan hoàn toàn 5,8 gam hỗn hợp gồm kim loại M và oxit của nó vào nước, thu được 1 lít dung dịch chứa một chất tan có nồng độ 0,04M và 0,448 lít khí H2 (đktc). Kim loại M là
A. Na
B. Ba
C. Ca.
D. K
Cho 2,3g Na tan hết trong 47,8ml nước thu được dung dịch NaOH và có khí H2 thoát ra. Tính nồng độ % của dung dịch NaOH?
\(n_{Na}=\dfrac{2.3}{23}=0,1\left(mol\right)\)
PTHH : 2Na + 2H2O -> 2NaOH + H2
0,1 0,1 0,1 0,05
\(m_{NaOH}=0,1.40=4\left(g\right)\)
\(m_{H_2O}=47,8\left(g\right)\)
\(m_{H_2}=0,05.2=0,1\left(g\right)\)
\(m_{dd}=47,8+2,3-0,1=50\left(g\right)\)
\(C\%_{NaOH}=\dfrac{4}{50}.100\%=8\%\)
\(47,8ml=47,8g\)
\(n_{Na}=\dfrac{2,3}{23}=0,1mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,1 0,1 0,05 ( mol )
\(m_{NaOH}=0,1.40=4g\)
\(m_{dd}=2,3+47,8-0,05.2=50g\)
\(C\%_{NaOH}=\dfrac{4}{50}.100=14\%\)
Cho 2,3g Na tan hết trong 47,8ml nước thu được dung dịch NaOH và có khí H2 thoát ra. Tính nồng độ C% của dung dịch NaOH?
mH2O = 47,8 . 1 = 47,8 (g)
nH2O = 47,8/18
nNa = 2,3/23 = 0,1 (mol)
PTHH: 2Na + 2H2O -> 2NaOH + H2
0,1 ---> 0,1 ---> 0,1 ---> 0,05
mNaOH = 0,1 . 40 = 4 (g)
mH2 = 0,05 . 2 = 0,1 (g)
mdd (sau p/ư) = 47,8 + 2,3 - 0,1 = 50 (g)
C%NaOH = 4/50 = 8%
ĐỀ hỏi nồng độ mol hay nồng độ chất tan vậy, nếu hỏi nồng độ chất tan thì đề lỗi
cho Na vào 250g nước cất có chất khí thoát ra dung dịch có tính kiềm , có C%=15,64% tính mNa có pth: 2Na + 2H2O---->2NaOH + h2